������CDMO��ҵ ADCҩ����ҵ����������;��
2020-02-27 δ֪ admin
�� | ���
10��16�գ�ҩ��������������俹��ż��ҩ�ADC��ԭҺ���Ƽ�����DP3����ʽͶ��GMP��ҵ��������ͬʱ���㽭ҽҩ�ع��ӹ�˾������������ҵ������ս�Ժ�������֧�ֺ���ADCҩ��ARX788��III���ٴ��о������ģ��ҵ��������
ҽҩħ���Ӻ���˫���˽�����Ǽ̡�ҩƷ��������������������MAH��ҩƷ�������ɳ������ƶȣ��������ADCҩ��ĺ�������������������ΪARX788��ί�з����Ը�ҩ��ķ��ٴ��о����ٴ����顢���������к��о���������Ӧ��⼰�����봦���ȳе����Σ�ҩ����������ARX788III���ٴ���Ʒ������������ҵ������ż��ԭҺ���Ƽ���Ʒ����������
ADCҩ�↑��������������������
ADCҩ����������������ϸ���ĵ���¡���壨mAb����ϸ������ͨ�������ӣ�linker��ż���õ��������Ͻ�������ҩ�����˵����ĵ������Ժ;��仯��ҩ���ϸ�����ԣ��ܹ����ɱ������ϸ���Ļ��Ժͽ��ͷ������Զ��ԡ�
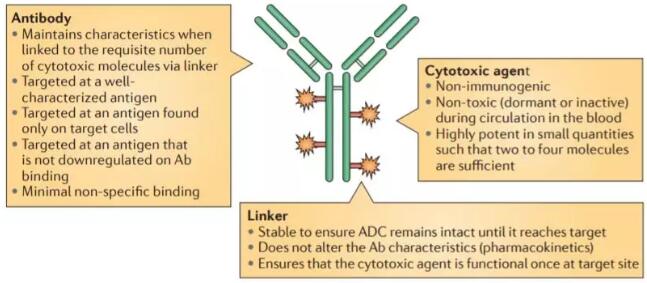
ADC�Ľṹ���������ԣ�ͼƬ��Դ��Nature Reviews Drug Discovery[1]��
���ڳ�����ҵ�������Ϊ�ڡ������ϼӵ�ͷ����ADCҩ��Ҳ����ҵ���������ﵼ������Ȼ����ADCҩ�����װȴ���Ǽؽ������붾��������������������ż�������ʮ�����ѡ�ADC�Ķ���һֱ�DZȽϴ����ս����Ҫ���������棬һ��ѭ��������ϸ�����ع����ͷţ����䣩����ɵ�ȫ�����ԣ�����ADC�������ܵ�����ԭ�ԡ����߶��Լ������ԡ�
Ŀǰ�����л����е�ADCҩ�ż����С���Ӷ��������ض�ż��λ���Dz�ȷ���ģ�����С���Ӷ���������ǰ���䣬��͵�����ADCҩ������ʵ�������еĸ���Ч�͵Ͷ��ԡ��������ﶭ�³����ܾ�����ѧ���ڽ��ܼ��߲ɷ�ʱ��ʾ��ARX788���Ӳ����˶��㡢�����Ͷ��ز����������п������ٴ��ϴ�����Ч�Ͷ����洦��
ADC�����漰���߶�С���ӵ�ʹ�ã�����ؼ����Լ���ȫ�������������ս��Ҫ�ḻ����������ʹ������豸Ͷ�ʣ���ˣ�ADCҩ���ż����������������������Ҫ��Ҳ��һ����Χ������ADCҩ����з���չ��
�г�������ã�ҩ��������ǰ����
2000��5�£�ȫ����ADCҩ��Mylotarg�������鵥���������ǣ���FDA���������У����������״θ�����60�����ϡ�CD33+�����ʺ�ϸ�������Ƶļ�������Ѫ����AML�����ߡ�Ȼ���ں������о��У���ҩ��δ���ֳ����Ե�������棬�������2010��6��������Mylotarg�������С���ʵ�ϣ���2017����ǰ��ADC�������ҩ����������Ծ��ȫ�����Adcetris��Kadcyla����ҩ�ﱻ�����С�
���Ŷ���ż�������ķ�չ���Լ�����Ч��С����ϸ�����غ������ƵĿ������μ����ij��֣�ADC��ҩ�з�������ů�������Mylotarg�ڳ���7������������У���ΪADC�������һ�ѻ�֮��3���µ�ADCҩ��½�����FDA������˹��������69����Ԫ�ӵ�һ������˾�ؽ��չ�trastuzumab deruxtecan����ҩ10��17����FDA�ݽ�BLA�������������������һϵ����ҵ�¼���ADCҩ���Ϊ���������ȳ������ҵ��ע����֮һ��
热词: